Trimetazidine bảo vệ cơ tim ở bệnh nhân lớn tuổi có bệnh mạch vành phải trải qua phẫu thuật ngoài tim: nghiên cứu ngẫu nhiên, mù đôi, có đối chứng với giả dược.
Người dịch: BS CKI Văn Minh Viên – BV Đa Khoa Vạn Hạnh
Zhong‑Liang Dai1,2*, Yi‑Feng Song1,2, Ya Tian1,2, Yin Li1,2, Miao Lin1,2, Juan Lin1,2, Qi Wang1,2, Ping Wang1,2 and Wen‑Li Gao1,2*
| Tóm tắt
Tổng quan: Điều trị trước đó với Trimetazidine đã cho thấy sự bảo vệ tế bào cơ tim trong phẫu thuật tim. TMZ có thể bảo vệ cho bệnh nhân lớn tuổi có bệnh tim thiếu máu cục bộ (IHD) phải trải qua phẫu thuật ngoài tim. Phương pháp: Nghiên cứu ngẫu nhiên, mù đôi, có đối chứng với giả dược (Số đăng kí #ChiCTR1900025018) thực hiên trên bệnh nhân lớn tuổi kèm IHD dự kiến phẫu thuật ngoài tim tại Bệnh viện Shenzhen People’s Hospital (tỉnh Quảng Đông, Trung Quốc) từ tháng 6 năm 2014 đến tháng 9 năm 2015, điều trị ngẫu nhiên với TMZ 60mg hoặc giả dược, uống 12 giờ trước phẫu thuật. Kết cục chính là sự xuất hiện của các biến cố tim mạch nội viện. Kết cục phụ là thiếu máu cơ tim cục bộ trên 5 chuyển đạo điện tâm đồ (cECG), tăng troponin I đặc hiệu tim (cTnI), tử vong tim mạch, biến cố vành cấp, suy tim và loạn nhịp tim cần điều trị. Kết quả: So với nhóm giả dược, nhóm điều trị với TMZ cho thấy tỉ lệ biến cố tim mạch nội viện thấp hơn (kết cục chính, 20.0% so với 37.5%, P= 0.02), tim thiếu máu cục bộ (15.0% so với 32.5%, P<0.01 ), tăng cTnI (2,5% so với 10%, P <0.01), biến cố mạch vành cấp tính (10.0% so với 20.0%, P <0.05), suy tim (0% so với 2.5%, P<0.05), và rối loạn nhịp tim cần điều trị (17.5% so với 35.0%, P <0.05). Không có nhồi máu cơ tim cấp trong 30 ngày hậu phẫu. Kết luận: Ở bệnh nhân cao tuổi mắc IHD trải qua phẫu thuật ngoài tim, điều trị trước đó với TMZ có liên quan với hiệu quả bảo vệ cơ tim. Hồ sơ đăng kí nghiên cứu: Nghiên cứu được đăng ký tại http://www.chictr.org.cn/showproj.aspx?proj=41909 với số đăng kí [ChiCTR1900025018] (7/8/2019). |
Tổng quan
Bệnh tim mạch, đặc biệt là Nhồi máu cơ tim cấp, đã và đang tăng lên trong 10 năm qua [1]. Tốc độ gia tăng của bệnh lý này trong dân số trên 65 tuổi nhanh hơn rất nhiều so với dân số chung. Tiền sử bệnh tim thiếu máu cục bộ (IHD) là một yếu tố nguy cơ của các biến cố tim mạch hậu phẫu, và tỉ lệ biến cố tim mạch nghiêm trọng có ý nghĩa lâm sàng mới mắc sau phẫu thuật ngoài tim lên đến 2.43% [3]. Đối với những người mắc IHD, các biến chứng chu phẫu của phẫu thuật ngoài tim khác nhau, từ loạn nhịp tim đến suy tim [4]. Các bác sĩ gây mê sẽ phải tham gia các phẫu thuật tự chọn hoặc phẫu thuật cấp cứu ở bệnh nhân cao tuổi được chẩn đoán xác định hoặc nghi ngờ mắc IHD. Nhiều bệnh nhân bị tổn thương cơ tim không triệu chứng trong quá trình phẫu thuật. Tổn thương cơ tim chu phẫu làm tăng tỷ lệ tử vong trong vòng 30 ngày gấp 10 lần [5]. Vì vậy, những bệnh nhân này cần được áp dụng các biện pháp an toàn và hữu hiệu để phòng ngừa tổn thương cơ tim.
Nhiều bằng chứng cho thấy IHD có thể được quản lý tốt [6, 7]. Mấu chốt là phải cân bằng nhu cầu và cung cấp oxy cho tế bào cơ tim [8]. Trimetazidine (1-[2,3,4-trimethoxybenzyl] piperazine dihydrochloride; TMZ) là một chất chống thiếu máu cục bộ nổi tiếng được sử dụng trong bảo vệ cơ tim [9]. Sử dụng TMZ tiền phẫu dường như có tác dụng tích cực đối với tình trạng bảo tồn cơ tim ở những bệnh nhân bắc cầu động mạch vành (CABG) [10]. Ngoài ra, gần đây, TMZ đã được sử dụng trong liệu pháp chuyển hóa để tối ưu hóa việc sử dụng năng lượng của cơ tim [11]. Hầu hết nghiên cứu tập trung vào cơ chế phân tử: Zhong và cộng sự [12] đã phát hiện rằng TMZ bảo vệ chống lại tổn thương do thiếu máu cục bộ / tái tưới máu (I / R) bằng cách cải thiện quá trình tự thực bào cơ thông qua con đường AMPK. Liu và cộng sự [13] phát hiện rằng TMZ ức chế quá trình apoptosis tế bào cơ tim do mạch vành nhỏ bị tắc nghẽn. Danikiewicz và cộng sự [14] cho thấy rằng điều trị với TMZ dẫn đến giảm mức IL-2 và IL-8 trước khi kiểm tra với máy chạy bộ. Con đường Nrf2/NF-κB trong tế bào cơ tim có thể là một cơ chế cho thấy tác dụng của TMZ đã đề cập ở trên [15].
Mặc dù hiệu quả bảo vệ tim mạch của TMZ đã được thừa nhận rõ ràng [16, 17], vẫn chưa rõ liệu có thể thấy được tác dụng bảo vệ này trong phẫu thuật ngoài tim hay không. Vì vậy, mục tiêu của nghiên cứu là để xác nhận hiệu quả bảo vệ của TMZ với người cao tuổi mắc IHD có trải qua phẫu thuật ngoài tim.
Phương pháp
Thiết kế nghiên cứu và đối tượng tham gia
Đây là một nghiên cứu ngẫu nhiên, mù đôi, có đối chứng với giả dược được phê duyệt bởi Ủy ban Đạo đức Shenzhen People’s Hospital, Quảng Đông, Trung Quốc (Chủ tịch là Giáo sư MJ. Tang, Ủy ban Đạo đức Số LL-KT-2014028). Tất cả các đối tượng đã được thông báo về các rủi ro và thủ tục quy trình của nghiên cứu trước khi thu nhận. Tất cả đối tượng tham phải có sự đồng ý bằng văn bản. Thử nghiệm lâm sàng này đã được đăng ký (# ChiCTR1900025018). Tất cả các phương pháp nghiên cứu đều phù hợp với bộ hướng dẫn và quy định có liên quan.
Tiêu chí thu nhận: bệnh nhân nam hoặc nữ (1) > 60 tuổi; (2) được chẩn đoán IHD theo tiêu chuẩn chẩn đoán bệnh mạch vành do Hiệp hội Tim mạch Hoa Kỳ công bố [18]; (3) phân độ II – IV theo Hiệp hội Bác sĩ gây mê Hoa Kỳ (ASA); (4) sẵn sàng tham gia và hoàn thành nghiên cứu; và (5) đã dự kiến cho các phẫu thuật lớn ngoài tim, như các thủ thuật mạch máu của động mạch chủ bụng hoặc chi dưới, các thủ thuật mở trong phúc mạc hoặc trong lồng ngực, và các thủ thuật chỉnh hình lớn dưới phần hông hoặc cột sống, và 1 số thủ thuật khác.
Tiêu chí loại trừ: (1) bệnh tim bẩm sinh, bệnh thấp tim, bệnh cơ tim, phì đại thất trái, hoặc bệnh van tim; (2) tiền sử nhồi máu cơ tim 3 tháng trước đó (3) rối loạn tâm thần; và (4) bất kỳ trường hợp từng dùng TMZ trước đó.
Ngẫu nhiên hóa và làm mù
Việc ngẫu nhiên hóa được thực hiện bằng cách sử dụng một bảng số ngẫu nhiên đã được lập trình sẵn bởi một nhà thống kê độc lập sử dụng SPSS 13.0 (SPSS Inc., Chicago, IL, USA). Trình tự ngẫu nhiên được chuẩn bị trong những phong bì niêm phong. Vào ngày trước phẫu thuật, một trong những nghiên cứu viên mang đến cơ sở y tế một chiếc phong bì ngẫu nhiên. Việc giấu kín được duy trì cho đến 12 giờ trước khi bắt đầu phẫu thuật, khi một y tá mở phong bì. Bệnh nhân, người thu thập dữ liệu và nhà phân tích dữ liệu được làm mù về loại thuốc được sử dụng. Vào ngày trước khi phẫu thuật, cả TMZ và giả dược (cùng màu sắc, kích thước và số lượng; 20 mg / viên) được chuyển đến y tá tại cơ sở y tế phụ trách bệnh nhân. Việc chuẩn bị và cấp phát thuốc được thực hiện bởi Y tá khoa phòng. Nghiên cứu viên dược làm mù để phân bổ việc điều trị.
Thuốc, gây mê và theo dõi
Tất cả bệnh nhân phải nhịn ăn 8-12 giờ trước phẫu thuật. Không dùng thuốc tiền mê. Thuốc đang dùng, chẳng hạn như thuốc chẹn β, ACEI, aspirin và statin, được tiếp tục uống cho đến sáng ngày phẫu thuật. Theo hướng dẫn sử dụng và các tài liệu tham khảo trước đó [9–11], 12 tiếng trước phẫu thuật, bệnh nhân uống thuốc theo sự hướng dẫn của Y tá(60 mg, ba viên, 20 mg/viên). Ngay khi bệnh nhân vào phòng phẫu thuật, việc theo dõi chuẩn được thực hiện: theo dõi 5 chuyển đạo ECG, đo oxy xung, huyết áp không xâm lấn, áp lực động mạch hướng tâm xâm lấn (chỉ thực hiện sau khi test Allen âm tính), nồng độ khí hít vào và thở ra, và sóng điện não (Máy theo dõi Chỉ số lưỡng phổ để đánh giá độ mê Bispectrial Index Monitor, Covidien, Dublin, Ireland). Dung dịch Ringer truyền với tốc độ 4ml/giờ đóng vai trò như tiền tải.
Tất cả các bệnh nhân đều được gây mê kết hợp qua đường tĩnh mạch / đường hít. Gây mê bằng midazolam 0,02 mg/kg, etomidate 0,3 mg/kg, cisatracurium 0,25 mg/ kg, và fentanyl citrate 3 µg/kg. Ngay khi vắng phản xạ mí mắt, thông khí hỗ trợ bằng mặt nạ thở với 100% oxy. Sau 5 phút khử nitơ, bằng oxy, thực hiên đặt nội khí quản (kích thước của ống thông là 7,5 # đối với nam và 7,0 # đối với nữ). Điều chỉnh các thông số máy thở (thể tích khí lưu thông 5–6 ml/kg, nhịp thở 12–16/phút) để duy trì nồng độ CO2 cuối thì thở ra (ETCO2) trong khoảng 35 đến 45 mmHg. Tong lúc phẫu thuật, duy trì gây mê bằng sevoflurane, propofol 2 mg/kg/h, remifentanil 0,15 µg/kg/phút, và liều bolus cisatracurium 0,03 mg/kg nếu cần. Duy trì thể tích dịch bằng dung dịch Ringer’s và dịch truyền hydroxyetyl starch. Độ sâu gây mê được điều chỉnh theo dấu hiệu sinh tồn và chỉ số lưỡng phổ (BIS) sao cho chỉ số tối ưu được duy trì trong khoảng từ 45 đến 60. Huyết áp trung bình và nhịp tim được duy trì ở mức ± 20% so với ban đầu. Ngưng Sevoflurane 15 phút trước khi kết thúc phẫu thuật, và lưu lượng oxy được tăng lên 5 l/phút để làm mới phổi, đồng thời tăng liều propofol để duy trì độ sâu gây mê thích hợp. Khi phẫu thuật kết thúc, ngưng tất cả các thuốc và bắt đầu giảm đau tĩnh mạch. Hút hết các dịch tiết trong khí quản và miệng. Rút nội khí khi bệnh nhân hồi phục phản xạ nuốt, thở tự phát và có thể đáp ứng. Sau khi rút ống thông động mạch hướng tâm, bệnh nhân được đưa về khoa.
Mẫu máu
Mẫu máu được thu thập trước và sau ca phẫu thuật, gồm 1 ml máu động mạch để phân tích khí máu và 3 ml máu tĩnh mạch. Lấy máu tĩnh mạch (3 ml) 24 và 48 giờ sau phẫu thuật.
Thu thập dữ liệu
Việc thu thập dữ liệu tiền phẫu bao gồm giới tính, tuổi, chỉ số khối cơ thể (BMI), Chỉ số nguy cơ tim mạch điều chỉnh của Lee, phân độ và mức độ của bệnh động mạch vành, phân loại NYHA, phân loại ASA và các thuốc tiền phẫu. Việc thu thập dữ liệu trong phẫu thuật bao gồm loại phẫu thuật, lượng máu mất, thời gian phẫu thuật, nồng độ trung bình sevoflurane hít vào , tốc độ truyền propofol trung bình, lượng remifentanil toàn phần trung bình trong phẫu thuật, giá trị BIS. Dữ liệu hậu phẫu là tình trạng thiếu máu cơ tim cục bộ trên 5 chuyển đạo ECG (ECG); nhồi máu cơ tim cấp (AMI); loạn nhịp tim trên lâm sàng, bao gồm rung nhĩ và block nhánh, nhịp nhanh thất, rung thất, hoặc bất kỳ tình trạng loạn nhịp nào ảnh hưởng đến huyết áp và cần điều trị; thời gian nằm khoa ICU; thời gian nằm viện(LOS); tái phẫu thuật trong thời gian nằm viện; và bất kỳ biến cố bất lợi nào khác. Chẩn đoán AMI dựa trên sự gia tăng troponin I đặc hiệu tim (cTnI) > 0,3 ng/ml sau phẫu thuật kèm ít nhất một trong các tiêu chí sau: (1) các triệu chứng thiếu máu cục bộ; (2) những thay đổi mới trên điện tâm đồ chỉ ra tình trạng thiếu máu cục bộ (thay đổi ST và/hoặc sóng T hoặc block nhánh trái được cho là mới khởi phát gần đây); và (3) sự phát triển của sóng Q bệnh lý trên điện tâm đồ. Điện tâm đồ được thu thập bởi một nghiên cứu viên độc lập không tham gia vào quá trinh điều trị bệnh. 30 ngày sau phẫu thuật, thu thập các dữ liệu về tử suất, AMI, loạn nhịp tim, rối loạn chức năng tim, tái nhập viện, và bất kỳ biến cố bất lợi nào khác. Thực hiện một cuộc phỏng vấn qua điện thoại với bệnh nhân và gia đình bệnh nhân. Tất cả dữ liệu đều được thu thập bởi các nghiên cứu viên không tham gia vào quá trình chăm sóc bệnh nhân.
Kết cục
Kết cục chính là các biến cố tim mạch nội viện. Các biến cố này bao gồm: AMI, các thay đổi mới và đáng kể trên sóng T cộng với đoạn ST (ST-T) hoặc block nhánh trái (LBBB), sự phát triển của sóng Q bệnh lý trên ECG, bằng chứng mới mất tế bào cơ tim trên hình ảnh học và bất kì bằng chứng về bất thường chuyển động vùng RWMA do huyết khối trong mạch vành qua chụp mạch hoặc khám nghiệm tử thi. Kết cục phụ là tim thiếu máu cục bộ qua cECG, tăng cTnI (> 0.3 ng/mL), tử vong tim mạch, biến cố vành cấp, suy tim ( phân suất tống máu thất trái < 40%), và loạn nhịp tim cần điều trị.
Cỡ mẫu
Sử dụng các biến cố tim mạch nội viện để tính toán cỡ mẫu. Khác biệt 20% ( 20% so với 40%) giữa 2 nhóm được coi là có ý nghĩa trên lâm sàng, dựa trên các nghiên cứu khác [19-21]. Sử dụng sai số α là 5% và công suất thử nghiệm là 80%, phân tích công suất chỉ ra rằng sự khác biệt như vậy sẽ được phát hiện với cỡ mẫu n = 60 (hoặc 30 cho mỗi nhóm). Giả sử loss to follow-up (tạm dịch: mất đối tượng theo dõi) 20%, mỗi nhóm phải có 40 bệnh nhân tham gia nghiên cứu.
Phân tích thống kê
Các phân tích được thực hiện bằng SPSS 13.0 (SPSS Inc., Chicago, IL, USA). Dữ liệu liên tục đã được kiểm định phân phối chuẩn bằng cách sử dụng test Kolmogorov– Smirnov. Dữ liệu liên tục được báo cáo dưới dạng giá trị trung bình ± SD hoặc trung vị (khoảng trải giữa IQR). Sự khác biệt giữa các nhóm được đánh giá bằng cách sử dụng kiểm định t-student hoặc kiểm định Mann– Whitney U, theo độ phân phối. Bảng phân loại được trình bày dưới dạng phần trăm và được so sánh bằng kiểm định chi-bình phương hoặc Fisher, nếu phù hợp. Mức đạt ý nghĩa thống kê khi P <0,0
Kết quả
Đặc điểm bệnh nhân
Tổng cộng có 80 bệnh nhân được đưa vào nghiên cứu, và không có bệnh nhân nào bỏ giữa chừng. Bảng 1 dưới đây trình bày các đặc điểm của bệnh nhân. Không có sự khác biệt có ý nghĩa thống kê giữa hai nhóm.
Bảng 1: Đặc điểm bệnh nhân và dữ liệu trong phẫu thuật
| TMZ (n=40) | Placebo (Giả dược) n=40 | P | |
| Tuổi | 65±6 | 64±8 | 0.86 |
| Nam giới,n (%) | 28 (70.0) | 26 (65.0) | 0.92 |
| BMI (Kg/m2) | 26.3±3.2 | 26.2±3.3 | 0.74 |
| Phân loại NYHA, n (%) | |||
| I | 12 (30.0) | 13 (32.5) | 0.85 |
| II | 18 (45.0) | 19 (47.5) | 0.95 |
| III | 7 (17.5) | 6 (15.0) | 0.64 |
| IV | 3 (7.5) | 2 (5.0) | 0.35 |
| Phân loại ASA, n (%) | |||
| II | 6 (15.0) | 7 (17.5) | 0.64 |
| III | 30 (75.0) | 28 (70.0) | 0.76 |
| IV | 4 (10.0) | 5 (12.5) | 0.85 |
| Tiền sử hút thuốc, n (%) | 12 (30) | 10 (25) | 0.72 |
| Tiền sử rối loạn Lipid huyết, n (%) | 25 (62.5) | 21 (52.5) | 0.58 |
| Tiền sử tăng huyết áp, n (%) | 11 (27.5) | 13 (32.5) | 0.80 |
| Tiền sử bệnh động mạch vành, n (%) | 31 (77.5) | 32 (80.0) | 0.86 |
| Tiền sử can thiệp mạch vành qua da hoặc phẫu thuật bắc cầu động mạch vành cho bệnh động mạch vành, n (%) | 8 (20) | 9 (22.5) | 0.79 |
| Tiền sử đột quỵ, n (%) | 5 (12.5) | 4 (10.0) | 0.85 |
| Tiền sử đái tháo đường, n (%) | 10 (25.0) | 9 (22.5) | 0.75 |
| Tiền sử dùng thuốc, n (%) | |||
| Chẹn beta | 29 (72.5) | 31 (77.5) | 0.76 |
| ACEI/ARB | 30 (75.0) | 32 (80.0) | 0.82 |
| Statins | 26 (65.0) | 27 (67.5) | 0.89 |
| Insulin | 4 (10.0) | 3 (7.5) | 0.85 |
| Thuốc trị đái tháo đường, đường uống | 10 (25.0) | 11 (27.5) | 0.88 |
| Thuốc chống kết tập tiểu cầu | 16 (40) | 14 (35) | 0.74 |
| Loại phẫu thuật, n (%) | |||
| Phẫu thuật tổng quát lớn | 11 (27.5) | 15 (37.5) | 0.56 |
| Chỉnh hình lớn | 21 (52.5) | 19 (47.5) | 0.64 |
| Mạch máu lớn | 8 (20.0) | 6 (15.0) | 0.80 |
| Tăng troponin trước phẫu thuật, n (%) | 2 (5.0) | 3 97.5) | 0.45 |
| Thời gian phẫu thuật (phút) | 156±24 | 162±28 | 0.79 |
| Thể tích máu mất (ml) | 256±146 | 267±165 | 0.62 |
| Chỉ số lưỡng phổ (BIS) | 45±12 | 46±14 | 0.83 |
Biến cố tim mạch nội viện
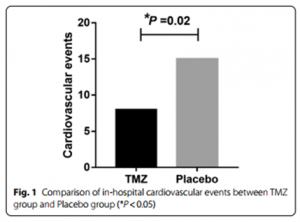
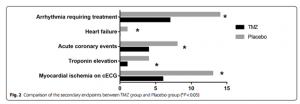
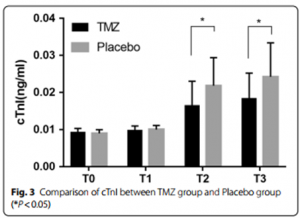
Hình 1 cho thấy có sự khác biệt giữa hai nhóm về kết cục chính (biến cố tim mạch) [8 (20.0%) so với. 15 (37.5%), P <0,05]. Hình 2 cho thấy kết cục phụ: loạn nhịp tim cần điều trị [7 (17.5%) so với 14 (35.0%), P <0.05] suy tim [0 so với 1 (2.5%), P <0.05], biến cố mạch vành cấp [4 (10.0%) so với 8 (20.0%), P <0.05]. tăng cTnI [1 (2.5%) so với 4 (10%), P <0.01]. và thiếu máu cơ tim cục bộ [6 (15.0 %) so với 13 (32.5%), P<0.01). Hình 3 cho thấy mức cTnI ở nhóm TMZ thấp hơn trong 24 giờ [0.0165 ± 0.0065 so với 0.0218 ± 0.0076] và 48 giờ sau phẫu thuật [0.0184 ± 0.0068 so với 0.0242 ± 0.0092].
Các biến cố trước phẫu thuật
Bảng 2 cho thấy không có sự khác biệt có ý nghĩa thống kê giữa hai nhóm về mê sảng (10.0% so với 12.5%, P= 0.15). tỷ lệ buồn nôn và nôn sau phẫu thuật (12.5% so với 15.0%, P= 0.45). hoặc thời gian nằm viện (7±1 so với 9 ± 1 ngày, P= 0.20). So với nhóm chứng. nhóm TMZ có thời gian nằm khoa ICU ngắn hơn (10 ± 2 so với 14 ± 1 giờ. P= 0.04). nhưng tỷ lệ bệnh nặng nội viện và tử suất cao hơn (5.0% so với 2.0%, P<0.05).
Kết quả của bệnh nhân trong 30 ngày sau phẫu thuật
Bảng 3 cho thấy kết cục trong 30 ngày của bệnh nhân. Không có sự khác biệt giữa hai nhóm về tử vong (7.5% so với 10.0%, P=0.10), phân độ suy tim theo NYHA (P > 0.05), rối loạn chức năng tim (5.0% so với 5.0%, P > 0.99), hoặc tái nhập viện (20.0% so với 25.0%, P=0.45). Không xuất hiện nhồi máu cơ tim cấp tính trong 30 ngày hậu phẫu. Tỉ lệ loạn nhịp tim thấp hơn ở nhóm TMZ so với nhóm chứng (15.0% so với 25.0%, P<0.05)
Hình 1: So sánh các biến cố tim mạch nội viên giữa nhóm TMZ và nhóm giả dược (*P<0.05)
Hình 2: So sánh kết cục phụ giữa nhóm TMZ và nhóm giả dược (*P<0.05)
Hình 3: So sánh Troponin I đặc hiệu tim giữa nhóm TMZ và nhóm giả dược (*P<0.05)
|
Bảng 2: Dữ liệu hậu phẫu
|
|||
|
|
TMZ (n=40) |
Placebo (n=40) |
P |
| Mê sảng, n (%) | 4 (10.0) | 5 (12.5) | 0.15 |
| Buồn nôn và nôn mới mắc hậu phẫu. | 5 (12.5) | 6 (15.0) | 0.45 |
| Thời gian nằm khoa ICU, số giờ trung bình (SD) | 10 (2) | 14 (1) | 0.04 |
| Tỉ lệ mắc bệnh và tử vong nội viện | 2 (5.0) | 1 (2.0) | < 0.05 |
| Thời gian nằm viện, số ngày, trung bình (SD) | 7 (1) | 9 (1) | 0.20 |
Bảng 3: Diễn biến lâm sàng trong 30 ngày hậu phẫu
| TMZ (n=40) |
Placebo (n=40) |
P | |
| Tử vong, n (%) | 3 (7.5) | 4 (10.0) | 0.10 |
| NYHA, n (%) | |||
| I | 13 (32.5) | 14 (35.0) | 0.65 |
| II | 19 (47.5) | 18 (45.0) | 0.55 |
| III | 6 (15.0) | 5 (12.5) | 0.45 |
| IV | 2 (5.0) | 3 (7.5) | 0.10 |
| AMI, n (%) | 0 | 0 | – |
| Loạn nhịp tim cần điều trị, n (%) | 6 (15.0) | 10 (25.0) | 0.02 |
| Rối loạn chức năng tim, n (%) | 2 (5.0) | 2 (5.0) | 0.99 |
| Tái nhập viện, n (%) | 8 (20.0) | 10 (25.0) | 0.45 |
Bàn luận
Điều trị trước đó với TMZ giúp bảo vệ tế bào cơ tim trong phẫu thuật tim [22, 23], nhưng dữ liệu về thuốc này trong phẫu thuật ngoài tim còn hạn chế. Vì vậy, nghiên cứu ngẫu nhiên, mù đôi có đối chứng này được thực hiện nhằm xác nhận hiệu quả bảo vệ của TMZ ở bệnh nhân cao tuổi mắc IHD phải trải qua phẫu thuật ngoài tim. Kết quả cho thấy ở những bệnh nhân này, điều trị trước đó với TMZ có liên quan đến hiệu quả bảo vệ cơ tim. TMZ có thể sử dụng để bảo vệ cơ tim bằng cách cân bằng nhu cầu và cung cấp oxy cũng như việc sử dụng năng lượng của cơ tim [21]. TMZ phòng ngừa tổn thương I/R bằng cách cải thiện quá trình tự thực bào ở tế bào cơ tim [12]. Các thử nghiệm lâm sàng trước đây cho thấy TMZ cải thiện chức năng cơ tim ở bệnh nhân bệnh mạch vành ổn định [19], cũng như ở bệnh nhân đã làm phẫu thuật bắc cầu động mạch vành (CABG) [22]. TMZ làm giảm các dấu hiệu viêm nhiễm trong quá trình kiểm tra trên thảm chạy [14]. Ở những bệnh nhân tiểu đường trải qua giai đoạn can thiệp động mạch vành qua da (PCI), TMZ làm giảm các chỉ dấu liên quan đến tổn thương tim và gan và giúp cải thiện chức năng tim [24]. Mặt khác, Costa và cộng sự [25] cho thấy TMZ không bổ sung bất kỳ lợi ích nào để điều hòa tiền thiếu máu cục bộ (IPC) ở bệnh nhân có bệnh động mạch vành ổn định. Trong nghiên cứu này, TMZ làm giảm các biến cố tim mạch nội viện (20.0% so với 37.5%) TMZ ở bệnh nhân cao tuổi mắc IHD phải trải qua phẫu thuật ngoài tim. Sự khác biệt giữa các nghiên cứu có thể là do quá trình chọn lọc bệnh nhân. Nghiên cứu hiện tại được hỗ trợ bởi các nghiên cứu trước đó, các nghiên cứu này đã cho thấy lợi ích từTMZ trên dân số đã chọn như bệnh nhân suy tim và bệnh động mạch ngoại biên [24], bệnh nhân đau thắt ngực ổn định [26], những người đang trải qua PCI [22], và những người bị suy tim mạn [27]. Các nghiên cứu bổ sung là không cần thiết để xác định bệnh nhân nào có thể được hưởng lợi nhiều nhất từ TMZ. Cũng giống như các biến cố tim mạch nội viện (kết cục chính), khác biệt có ý nghĩa thống kê cũng được quan sát thấy qua kết cục phụ giữa hai nhóm, như thiếu máu cơ tim cục bộ, tăng cTnI, biến cố vành cấp, suy tim và loạn nhịp tim cần điều trị. Một lần nữa, điều này đã được chứng minh bởi các nghiên cứu trước đây thực hiện trên nhiều đối tượng bệnh nhân [24, 26]. Trong nghiên cứu này, không có biến cố bất lợi liên quan đến TMZ được quan sát. Ngoài ra, không có sự khác biệt giữa hai nhóm về tình trạng mê sảng hoặc buồn nôn và nôn mới mắc sau phẫu thuật. Kết quả cho thấy tính an toàn của TMZ là tốt, như được báo cáo bởi các nghiên cứu trước đây [28]. Chảy máu nặng là một nguy cơ đáng quan tâm sau PCI, nhưng nguy cơ xuất huyết giữa hai nhóm không có nghĩa nghĩa thống kê [29, 30].
Tại thời điểm 30 ngày hậu phẫu, không có sự khác biệt giữa hai nhóm về tỷ lệ tử vong, rối loạn chức năng tim, tái nhập viện hoặc phân độ suy tim theo NYHA. Điều này có thể là do ngay cả khi bệnh nhân mắc IHD, bệnh lý IHD này không phải là lý do để phẫu thuật, có nghĩa là IHD của họ đã được kiểm soát tương đối tốt, che lấp những lợi ích tiềm năng trung hạn của TMZ trên những bệnh nhân đó. Tuy nhiên, tình trạng loạn nhịp tim thấp hơn ở nhóm TMZ, cho thấy rằng những bệnh nhân này có thể nhận được một số lợi ích từ TMZ trong thời gian dài hơn. Các nghiên cứu bổ sung là cần thiết để kiểm tra điều này.
Thử nghiệm này vẫn có những hạn chế. Đầu tiên, do khả năng phòng thí nghiệm còn hạn chế, chúng tôi không thể kiểm tra các cơ chế phân tử chính xác của TMZ. Thứ hai, như đã trình bày ở trên, có nhiều khả năng có thể xảy ra khi mà TMZ hoạt động như một chất bảo vệ cơ tim. Thứ ba, đây là một thử nghiệm đơn trung tâm, mẫu nhỏ, vì vậy khả năng khái quát hóa các kết luận trong nghiên cứu này còn bị hạn chế. Các nghiên cứu quy mô lớn là cần thiết để làm rõ hiệu quả của việc điều trị trước với TMZ trên dân số mục tiêu.
Kết luận
Tóm lại, ở bệnh nhân cao tuổi mắc IHD phải trải qua phẫu thuật ngoài tim, điều trị trước với TMZ có liên quan đến tác dụng bảo vệ cơ tim.
Viết tắt
TMZ: Trimetazidine; IHD: Bệnh tim thiếu máu cục bộ; cTnI: Troponin I đặc hiệu tim; ASA: Hiệp hội bác sĩ gây mê Hoa Kỳ; BIS: Chỉ số lưỡng phổ; BMI: Chỉ số khối cơ thể; ECG: Điện tâm đồ; AMI: Nhồi máu cơ tim cấp; LOS: thời gian nằm viện.
Lời cảm ơn
Các tác giả xin cảm ơn Tiến sĩ Haibo Wang từ Đại học Bắc Kinh về việc chuẩn bị thống kê. Chúng tôi cũng cảm ơn Giáo sư Zhengyuan Xia từ Đại học Hồng Kông đã hỗ trợ trong việc chuẩn bị bản thảo. Các tác giả cảm ơn Zhongjun Zhang, Xueping Zhang và Dengfeng Ding vì vai trò quan trọng của họ trong việc tuyển dụng bệnh nhân và thu thập dữ liệu.
Đóng góp của các tác giả
ZD, WG và PW đã thực hiện các nghiên cứu, tham gia thu thập dữ liệu và soạn thảo bản thảo. YS, YT và ML đã thực hiện phân tích thống kê và tham gia vào thiết kế của nó. QW, JL và YL đã tham gia vào việc thu thập, phân tích hoặc giải thích dữ liệu và soạn thảo bản thảo. Tất cả các tác giả đã đọc và chấp thuận bản thảo cuối cùng.
Tài trợ
Nghiên cứu này được tài trợ bởi Quỹ Khoa học và Công nghệ Thành phố Thâm Quyến (JCYJ20170307100314152), Quỹ Nghiên cứu Sức khỏe Thâm Quyến (SZLY2018011; SZXJ2017029), Quỹ Nghiên cứu Y tế Quảng Đông (A2018008; A2019382) và Quỹ Nghiên cứu Khoa học Khoa học của Bệnh viện Nhân dân Thâm Quyến (SYLY201706).
Tính sẵn có của dữ liệu và tài liệu
Tất cả dữ liệu được tạo ra hoặc phân tích trong quá trình nghiên cứu này đều được bao gồm trong bản thảo này và phần bổ sung của nó.
Tuyên bố
Phê duyệt và đồng ý tham gia
Nghiên cứu này đã được phê duyệt bởi Ủy ban Đạo đức Bệnh viện Nhân dân Thâm Quyến, Quảng Đông, Trung Quốc (Chủ tịch Giáo sư MJ. Tang, Ủy ban Đạo đức Số LL-KT-2014028). Tất cả các đối tượng đã được thông báo thích hợp về các rủi ro và quy trình của nghiên cứu trước khi ghi danh. Tất cả những người tham gia với điều kiện có sự đồng ý bằng văn bản thông báo.
Đồng ý xuất bản
Không áp dụng.
Các lợi ích cạnh tranh
Các tác giả tuyên bố rằng họ không có lợi ích cạnh tranh.
Thông tin chi tiết về tác giả
1Khoa Gây mê, Bệnh viện Nhân dân Thâm Quyến (The Second Medical College, Jinan University; The First Afliated Hospital, Southern University of Science and Technology), Thâm Quyến 518020, Quảng Đông, Trung Quốc. 2Trung tâm Nghiên cứu Kỹ thuật gây mê Thâm Quyến, số 1017 Dong‑ men North Road, Thâm Quyến 518020, Quảng Đông, Trung Quốc.
Đã nhận: ngày 21 tháng 5 năm 2021 Được chấp nhận: ngày 24 tháng 9 năm 2021
- Arnett DK, Blumenthal RS, Albert MA, Buroker AB, Goldberger ZD, Hahn EJ, et al. 2019 ACC/AHA guideline on the primary prevention of cardiovascular disease: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation. 2019;140:e596–e646.
- Belli R, Bonato A, De Angelis L, Mirabilii S, Ricciardi MR, Tafuri A, et al. Metabolic reprogramming promotes myogenesis during aging. Front Physiol. 2019;10:897. doi: 10.3389/fphys.2019.00897.
- Chapman AR, Adamson PD, Shah ASV, Anand A, Strachan FE, Ferry AV, et al. High-sensitivity cardiac troponin and the universal definition of myocardial infarction. Circulation. 2020;141:161–171. doi: 10.1161/CIRCULATIONAHA.119.042960.
- Chen J, Wang B, Lai J, Braunstein Z, He M, Ruan G, et al. Trimetazidine attenuates cardiac dysfunction in endotoxemia and sepsis by promoting neutrophil migration. Front Immunol. 2018;9:2015. doi: 10.3389/fimmu.2018.02015.
- Chrusciel P, Rysz J, Banach M. Defining the role of trimetazidine in the treatment of cardiovascular disorders: some insights on its role in heart failure and peripheral artery disease. Drugs. 2014;74:971–980. doi: 10.1007/s40265-014-0233-5.
- Costa LMA, Rezende PC, Garcia RMR, Uchida AH, Seguro L, Scudeler TL, et al. Role of trimetazidine in ischemic preconditioning in patients with symptomatic coronary artery disease. Medicine. 2015;94:e1161. doi: 10.1097/MD.0000000000001161.
- Dalal JJ, Mishra S. Modulation of myocardial energetics: an important category of agents in the multimodal treatment of coronary artery disease and heart failure. Indian Heart J. 2017;69:393–401. doi: 10.1016/j.ihj.2017.04.001.
- Danikiewicz A, Szkodziński J, Hudzik B, Korzonek-Szlacheta I, Gąsior M, Zubelewicz-Szkodzińska B. Effects of trimetazidine on interleukin-2 and interleukin-8 concentrations in patients with coronary artery disease. Can J Physiol Pharmacol. 2017;95:759–762. doi: 10.1139/cjpp-2016-0424.
- Fellahi JL, Godier A, Benchetrit D, Berthier F, Besch G, Bochaton T, et al. Perioperative management of patients with coronary artery disease undergoing non-cardiac surgery: summary from the French Society of Anaesthesia and Intensive Care Medicine 2017 convention. Anaesthesia Crit Care Pain Med. 2018;37:367–374. doi: 10.1016/j.accpm.2018.02.021.
- Ferguson MT, Hofman MS, Ismail H, Melville A, Yap KSK, Hicks RJ, et al. A pilot study of cardiopulmonary exercise testing and cardiac stress positron emission tomography before major non-cardiac surgery. Anaesthesia. 2018;73:1524–1530. doi: 10.1111/anae.14447.
- Glezer M. The Effectiveness of trimetazidine treatment in patients with stable angina pectoris of various durations: results from the CHOICE-2 study. Adv Ther. 2018;35:1103–1113. doi: 10.1007/s12325-018-0674-4.
- Liu YC, Li L, Su Q, Liu T, Tang ZL. Trimetazidine pretreatment inhibits myocardial apoptosis and improves cardiac function in a Swine model of coronary microembolization. Cardiology. 2015;130:130–136. doi: 10.1159/000369246.
- Marzilli M, Vinereanu D, Lopaschuk G, Chen Y, Dalal JJ, Danchin N, et al. Trimetazidine in cardiovascular medicine. Int J Cardiol. 2019;293:39–44. doi: 10.1016/j.ijcard.2019.05.063.
- Meiszterics Z, Kónyi A, Hild G, Sárszegi Z, Gaszner B. Effectiveness and safety of anti-ischemic trimetazidine in patients with stable angina pectoris and type 2 diabetes. J Compar Effect Res. 2017;6:649–657. doi: 10.2217/cer-2017-0011.
- Sellers D, Srinivas C, Djaiani G. Cardiovascular complications after non-cardiac surgery. Anaesthesia. 2018;73(Suppl 1):34–42. doi: 10.1111/anae.14138.
- Sistino JJ, Fitzgerald DC. Epidemiology of cardiovascular disease in the United States: implications for the perfusion profession. A 2017 update. Perfusion. 2017;32:501–506. doi: 10.1177/0267659117696140.
- Su Q, Li L, Zhao J, Sun Y, Yang H. Effects of Trimetazidine on PDCD4/NF-κB/TNF-α pathway in coronary microembolization. Cell Physiol Biochem Int J Exp Cell Physiol Biochem Pharmacol. 2017;42:753–760. doi: 10.1159/000478067.
- Tarkin JM, Kaski JC. Trimetazidine: is there a role beyond angina? Eur Heart J Cardiovasc Pharmacother. 2018;4:67–68. doi: 10.1093/ehjcvp/pvx029.
- Thadani U. Trimetazidine for stable and unstable ischemic heart diseases and for heart failure: is its routine use justified from available data? Int J Cardiol. 2020;300:45–46. doi: 10.1016/j.ijcard.2019.07.093.
- Tsioufis K, Andrikopoulos G, Manolis A. Trimetazidine and cardioprotection: facts and perspectives. Angiology. 2015;66:204–210. doi: 10.1177/0003319714530040.
- Tuunanen H, Engblom E, Naum A, Någren K, Scheinin M, Hesse B, et al. Trimetazidine, a metabolic modulator, has cardiac and extracardiac benefits in idiopathic dilated cardiomyopathy. Circulation. 2008;118:1250–1258. doi: 10.1161/CIRCULATIONAHA.108.778019.
- Valle JA, Graham L, Thiruvoipati T, Grunwald G, Armstrong EJ, Maddox TM, et al. Facility-level association of preoperative stress testing and postoperative adverse cardiac events. Heart (British Cardiac Society) 2018;104:2018–2025.
- Volgman AS, Palaniappan LS, Aggarwal NT, Gupta M, Khandelwal A, Krishnan AV, et al. Atherosclerotic Cardiovascular Disease in South Asians in the United States: Epidemiology, Risk Factors, and Treatments: A Scientific Statement From the American Heart Association. Circulation. 2018;138:e1–e34. doi: 10.1161/CIR.0000000000000580.
- Yaman M, Arslan U, Gümrükçüoğlu HA, Şahin M, Şimşek H, Akdağ S. Effects of Trimetazidine on T Wave Alternans in Stable Coronary Artery Disease. Korean circulation journal. 2016;46:343–349. doi: 10.4070/kcj.2016.46.3.343.
- Zhang H, Liu M, Zhang Y, Li X. Trimetazidine attenuates exhaustive exercise-induced myocardial injury in rats via regulation of the Nrf2/NF-κB signaling pathway. Front Pharmacol. 2019;10:175. doi: 10.3389/fphar.2019.00175.
- Zhang L, Lu Y, Jiang H, Zhang L, Sun A, Zou Y, et al. Additional use of trimetazidine in patients with chronic heart failure: a meta-analysis. J Am Coll Cardiol. 2012;59:913–922. doi: 10.1016/j.jacc.2011.11.027.
- Zhang N, Lei J, Liu Q, Huang W, Xiao H, Lei H. The effectiveness of preoperative trimetazidine on myocardial preservation in coronary artery bypass graft patients: a systematic review and meta-analysis. Cardiology. 2015;131:86–96. doi: 10.1159/000375289.
- Zhong Y, Zhong P, He S, Zhang Y, Tang L, Ling Y, et al. Trimetazidine Protects Cardiomyocytes Against Hypoxia/Reoxygenation Injury by Promoting AMP-activated Protein Kinase-dependent Autophagic Flux. J Cardiovasc Pharmacol. 2017;69:389–397. doi: 10.1097/FJC.0000000000000487.
- Gragnano F, Spirito A, Corpataux N, Vaisnora L, Galea R, Gargiulo G, Siontis GCM, Praz F, Lanz J, Billinger M, Hunziker L, Stortecky S, Pilgrim T, Bär S, Ueki Y, Capodanno D, Urban P, Pocock SJ, Mehran R, Heg D, Windecker S, Räber L, Valgimigli M. Impact of clinical presentation on bleeding risk after percutaneous coronary intervention and implications for the ARC-HBR definition. EuroIntervention. 2021 doi: 10.4244/EIJ-D-21-00181.
- Urban P, Mehran R, Colleran R, Angiolillo DJ, Byrne RA, Capodanno D, Cuisset T, Cutlip D, Eerdmans P, Eikelboom J, Farb A, Gibson CM, Gregson J, Haude M, James SK, Kim HS, Kimura T, Konishi A, Laschinger J, Leon MB, Magee PFA, Mitsutake Y, Mylotte D, Pocock S, Price MJ, Rao SV, Spitzer E, Stockbridge N, Valgimigli M, Varenne O, Windhoevel U, Yeh RW, Krucoff MW, Morice MC. Defining high bleeding risk in patients undergoing percutaneous coronary intervention. Circulation. 2019;140(3):240–261. doi: 10.1161/CIRCULATIONAHA.119.040167.







Xin vui lòng đăng nhập để nhận xét vào bài viết này.